Giải SBT KHTN 7 cánh diều bài 1: Nguyên tử | SBT Khoa học tự nhiên 7 cánh diều
- Xác định khối lượng của hạt nhân nguyên tử boron chứa 5 proton, 6 neutron và khối lượng nguyên tử boron. So sánh hai kêt quả tính được và nêu nhận xét. | SBT Hoá học 10 Kết nối tri thức
- Giải SBT bài 13: Nước biển và đại dương | SBT Địa lí 10
- NATO là gì? NATO gồm những nước nào?
- Triết học cổ điển Đức là gì? Nội dung của triết học cổ điển Đức
- Khi tiến hành thí nghiệm chứng minh lá thoát hơi nước, nên chọn loại túi có đặc điểm gì để trùm lên lá?
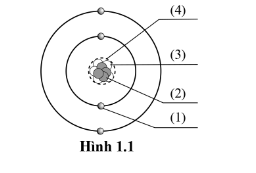
Bài tập 1.1 Gọi tên các thành phần của một nguyên tử (hạt nhân, proton, neutron, electron) được mô tả như hình 1.1 dưới đây.
Bạn đang xem: Giải SBT KHTN 7 cánh diều bài 1: Nguyên tử | SBT Khoa học tự nhiên 7 cánh diều

Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
- (1) Hạt nhân
- (2) Neutron
- (3) Proton
- (4) Electron
Bài tập 1.2 Quan sát hình 1.2, cho biết số proton, neutron, electron và điện tích hạt nhân của mỗi nguyên tử.

Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
|
Nguyên tử |
Số proton |
Số neutron |
Số electron |
Điện tích hạt nhân |
|
Boron |
5 |
6 |
5 |
+5 |
|
Fluorine |
9 |
10 |
9 |
+9 |
Bài tập 1.3. Hãy chọn từ/ cụm từ thích hợp cho sẵn dưới đây để điền vào chỗ trong mỗi câu sau: proton, neutron, electron, hạt nhân nguyên tử, vỏ nguyên tử, nguyên tử.
a) Trong nguyên tử, số proton bằng số …..
b) Hạt nhân nguyên tử gồm và …..
c) Phần lớn khối lượng nguyên tử tập trung ở …
d) Trong hạt nhân nguyên tử, hạt ….. không mang điện.
Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
a) Trong nguyên tử, số proton bằng số …electron….
b) Hạt nhân nguyên tử gồm và ..preoton, neutron…
c) Phần lớn khối lượng nguyên tử tập trung ở …hạt nhân nguyên tử….
d) Trong hạt nhân nguyên tử, hạt …neutron…. không mang điện.
Bài tập 1.4 Mỗi phát biểu sau là đúng hay sai?
a) Các hạt electron được tìm thấy trong hạt nhân của nguyên tử.
b) Các hạt neutron và electron hút nhau. c) Trong nguyên tử, số electron tối đa ở lớp electron thứ hai là 8.
d) Phần lớn khối lượng của nguyên tử tập trung ở hạt nhân nên kích thước của hạt nhân gần bằng kích thước của nguyên tử.
Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
a. Sai
b. Sai
c. Đúng
d. Sai
Bài tập 1.5 Chọn phát biểu đúng về electron.
- A. Một electron có khối lượng lớn hơn một proton và mang điện tích âm.
- B. Một electron có khối lượng nhỏ hơn một proton và mang điện tích âm. C. Một electron có khối lượng nhỏ hơn một neutron và không mang điện tích. D. Một electron mang điện tích dương và có khối lượng lớn hơn một neutron.
Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
Chọn đáp án B
Bài tập 1.6 Quan sát hình ảnh mô tả cấu tạo nguyên tử nitrogen và silicon (hình 1.3), cho biết mỗi nguyên tử đó có bao nhiêu lớp electron và số electron trên mỗi lớp electron đó.

Trả lời
- Nguyên tử nitrogen có 2 lớp electron. Số electron trên lớp thứ nhất và lớp thứ hai lần lượt là 2 và 5.
- Nguyên tử silicon có 3 lớp electron. Số electron trên lớp thứ nhất, lớp thứ hai và lớp thứ ba lần lượt là 2, 8 và 4.
Bài tập 1.7 Cho biết nguyên tử sulfur (lưu huỳnh) có 16 electron. Hãy vẽ sơ đồ mô tả sự phân bố electron trên các lớp electron của nguyên tử sulfur và cho biết mỗi lớp electron có bao nhiêu electron.
Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời

Bài tập 1.8 Hoàn thành bảng sau bằng cách điền thông tin thích hợp vào các ô trống:
|
Nguyên tử |
Số neutron |
số proton |
số electron |
khối lượng nguyên tử (anu) |
|
Argon |
10 |
10 |
|
|
|
Phosphorus |
|
1519 |
16 |
31 |
|
Sulfur |
16 |
|
|
|
|
Potassium |
|
|
|
39 |
Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
|
Nguyên tử |
Số neutron |
số proton |
số electron |
khối lượng nguyên tử (anu) |
|
Argon |
10 |
10 |
10 |
20 |
|
Phosphorus |
16 |
15 |
16 |
31 |
|
Sulfur |
16 |
16 |
15 |
21 |
|
Potassium |
20 |
19 |
19 |
39 |
Bài tập 1.9 Tổng số proton, neutron và electron của nguyên tử X là 46. Trong đó, mang điện nhiều hơn số hạt không mang điện là 14. a) Tính số proton, số neutron và số electron của nguyên tử X. hat
b) Tính khối lượng nguyên tử X.
c) Cho biết nguyên tử X có bao nhiêu lớp electron và chỉ ra số electron trên mỗi lớp.
Trả lời
a) Gọi số hạt proton, neutron và electron trong nguyên tử X lần lượt là P, N và E.
Ta có:
P+E+N=46 (1)
P+E N+14 (2)
P=E (3)
Từ (1), (2) và (3) => P = E = 15, N = 16. Vậy số hạt proton, neutron và electron của nguyên tử X lần lượt là 15, 16 và 15.
b) Khối lượng nguyên tử X là: P+ N = 15 + 16=31 (amu).
c) Vì X có 15 proton trong hạt nhân nên X là nguyên tử phosphorus.
Nguyên tử X (phosphorus) có 3 lớp electron.
Số electron trên lớp thứ nhất, lớp thứ hai và lớp thứ ba lần lượt là 2, 8 và 5.
Bài tập 1.10*
Tổng số proton, neutron và electron của nguyên tử X là 10.
a) Xác định số proton, số neutron và số electron của nguyên tử X. Biêt trong nguyên tử X, số neutron lớn hơn số electron và nhỏ hơn 1,5 lần số electron.
b) Xác định số đơn vị điện tích hạt nhân của X.
c) Tính khối lượng nguyên tử X.
d) Cho biết nguyên tử X có bao nhiêu lớp electron và xác định số electron ở lớp ngoài cùng của X.
Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
a. Gọi số proton và neutron trong nguyên tử X lần lượt là P và N.
Ta có: Tổng số proton, neutron và electron là:
A= 2P + N
Do P <N < 1,5 P nên 3P < S > 3,5 P
Suy ra:
$\frac{S}{3,5}$ < O < $\frac{S}{3}$
=> $\frac{10}{3,5}$ < P < $\frac{10}{3}$
=> 2,9 < P < 3,3
Do P là số nguyên nên P = 3 => N = 4
Vậy số hạt proton, neutron và electron của nguyên tử X lần lượt là 3,4 và 3
b. Số đơn vị điện tích hạt nhân của X là 3 (Vì X có 3 proton)
c. Khối lượng của nguyên tử X là: p+ n= 3 +4 + 7 ( amu)
d. Vì X có 3 proton trong hạt nhân nên X là nguyên tử lithium
Nguyên tử X (lithium) có 2 lớp electron. Số electron lớp ngoài cùng của X là 1
Bài tập 1.11
a) Khối lượng của nguyên tử A là 3 amu. a) Xác định số proton, số neutron và số electron của nguyên tử A, biết số electron nhỏ hơn số neutron. trong A,
b) Cho biết số electron lớp ngoài cùng của A.
Xem thêm : Taluy là gì? Taluy âm là gì? Taluy dương là gì?
Trả lời
a) Gọi số hạt proton, neutron và electron trong nguyên tử X lần lượt là P, N và E. Ta có khối lượng của nguyên tử A là P+N=3. Mà số electron lại nhỏ hơn số neutron, nghĩa là số proton nhỏ hơn số neutron.
P=1, N=2, E = 1
Vậy số hạt proton, neutron và electron của nguyên tử A lần lượt là 1, 2 và 1.
b) Số electron lớp ngoài cùng của A là 1.
Nguồn: https://thcshongthaiad.edu.vn
Danh mục: Tra Cứu
